Chimie et propriétés communes des céramiques et des verres
Microstructures et propriétés mécaniques des céramiques
Les verres
Les liants hydrauliques
La céramique est probablement le plus ancien matériau fabriqué par l’homme. L’ubiquité de ses matières premières, sa facilité de mise en forme et ses propriétés de tenue en température ont fait de ce matériau un marqueur de civilisation depuis la nuit des temps, partout à travers le monde. C’est grâce aux paniers et aux pots que les hommes ont pu commencer à stocker le grain et l’eau et cuire leurs aliments, passant ainsi la grande étape de la sédentarisation. Ces céramiques de la Préhistoire et de l’Histoire désignent les matériaux formés par la transformation thermique de poudres minérales, souvent des argiles, qui ont été mises en forme et compactées.

Idole en terre cuite de Dolni-Vestonice, 29000-25000 BC, première céramique connue actuellement.


(A gauche) Hippopotame en faïence archéologique, Egypte, 2000 BC, Musée du Louvre. (A droite) Vase de la nécropole de Suse, Mésopotamie, 4500-3500 BC, Musée du Louvre.
Après les premiers objets en terre cuite, deux voies ont été suivies en parallèle dans le développement de la céramique en Haute Antiquité. Les « faïences archéologiques » sont constituées de silice avec un peu de verre alcalin qui sert de liant. Les matières premières sont le sable ou la stéatite et des fondants. Elles sont développées surtout en Egypte et dans la vallée de l’Indus. Les « céramiques argileuses » ont pour principale matière première l’argile. Elles apparaissent en Mésopotamie et bien plus tard en Egypte et en Grèce. Il était plus facile de faire tenir une glaçure bleue sur une faïence siliceuse que sur une céramique argileuse, ce qui peut expliquer en partie ce décalage.
Le sens du mot céramique est beaucoup plus large aujourd’hui. Lorsqu’on classe les matériaux par familles, les céramiques sont l’ensemble des matériaux qui ne sont ni des métaux, ni des matériaux organiques. Dans ce sens, les verres minéraux et les liants hydrauliques comme le plâtre ou le ciment font partie de la famille. Mais si on ajoute la dimension des procédés, les céramiques restent ces matériaux obtenus par mise en forme et compactage de poudres minérales, suivis de leur densification par l’effet de la chaleur, un traitement thermique appelé frittage. Par contraste, les verres sont obtenus par la fusion complète du mélange de poudres, pour former un liquide qui est ensuite rapidement mis en forme et refroidi. Les liants hydrauliques, eux, sont obtenus en préparant par chauffage une poudre d’oxydes très réactive à l’eau (clinker, plâtre, chaux pour les principaux) qui va durcir en formant des hydrates, une fois mélangée à l’eau.
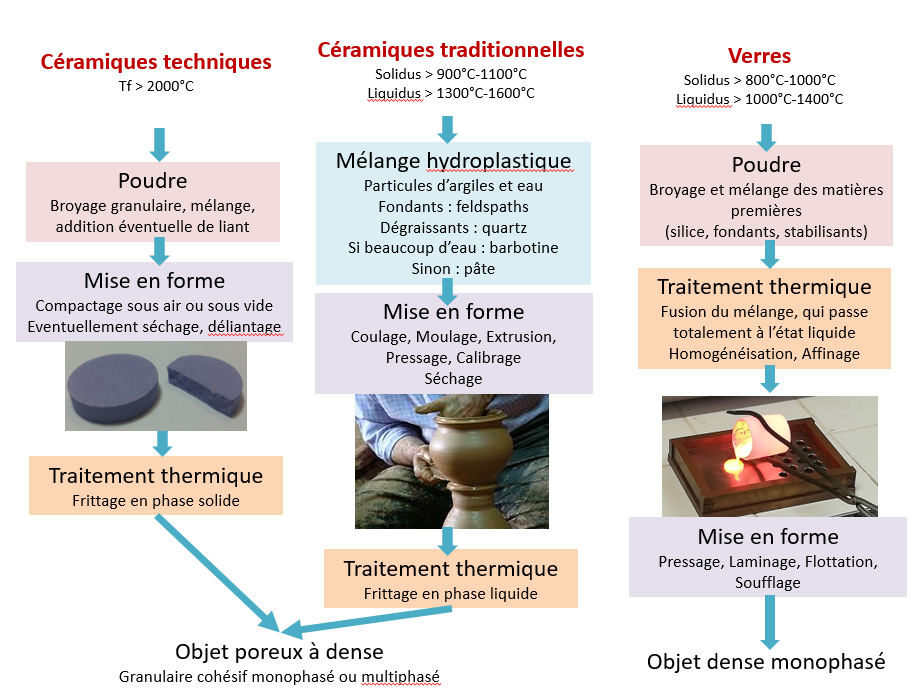
Les différences entre les procédés d’élaboration des céramiques et des verres
Les matériaux céramiques recouvrent essentiellement des matériaux à base d’oxydes, mais la chimie récente a élargi la famille à d’autres composés, tels que les borures, carbures, nitrures, oxynitrures, fluorures et oxyfluorures… Les céramiques à base de matières premières argileuses (la « terre ») sont appelées céramiques traditionnelles, par opposition aux céramiques techniques plus récentes. Une intense activité de recherche et développement porte sur les céramiques techniques, vaste champ où on distingue les céramiques fonctionnelles (utilisées pour leurs propriétés électroniques, optiques et magnétiques : par exemple Al2O3, BaTiO3, MnFe2O4…) et les céramiques structurales (utilisées pour leurs propriétés mécaniques à haute température : certains oxydes très réfractaires, les carbures, les nitrures…). Mais les céramiques traditionnelles dominent et domineront toujours le marché des céramiques, du fait de leurs applications de grande diffusion : carreaux de revêtement pour sols et murs, tuiles et briques, réfractaires, sanitaires, vaisselle, ornement… Ces céramiques nées dans la Préhistoire savent pourtant « rester dans le coup » car, par la voie de la pâte argileuse, elles se prêtent très bien à l’impression 3D. Les céramiques non argileuses s’y prêtent aussi, pourvu qu’on mélange la poudre à un liant. L’aventure continue!
Chimie et propriétés communes des céramiques et des verres
En tant que matériaux non organiques non métalliques, qui sont-elles, les céramiques?
Elles sont basées sur des composés formés d’un élément très électronégatif, comme l’oxygène, et d’un métal ou élément électropositif, comme Si, Al, Na, Ca, Ti, Fe, … (la gauche et le centre du tableau périodique). L’oxygène est l’anion O2-, les métaux sont les cations. Ces composés sont les oxydes, leur liaison chimique est de type iono-covalente et par conséquent, leur énergie interne est très élevée. Leur structure va de l’empilement d’anions et cations en interaction ionique, au réseau de petits polyèdres (par exemple le tétraèdre SiO4) lorsque la liaison est plus covalente.
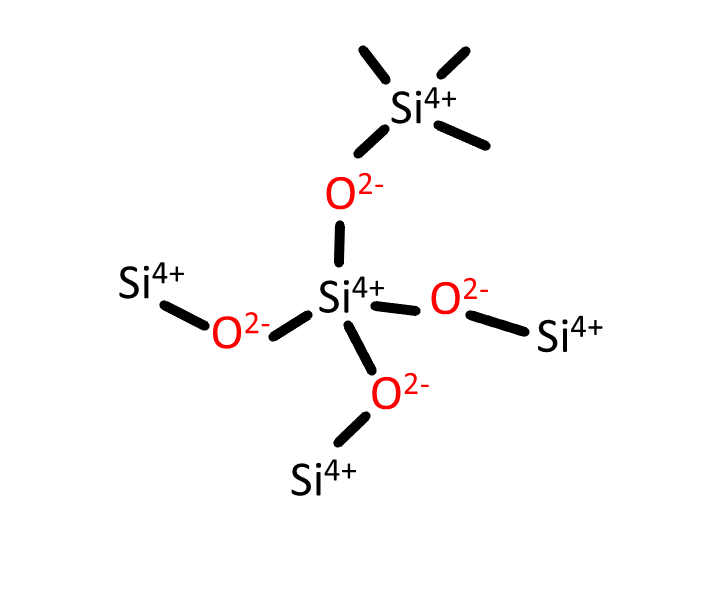

crédit : Markus Heyde/Fritz Haber, Max Planck Institute, DOI:https://doi.org/10.1103/PhysRevLett.109.106101
Exemple de la silice SiO2. La liaison Si-O est fortement ionique, mais aussi fortement covalente. La structure de la silice est formée de l’enchaînement de tétraèdres SiO4 dont les liaisons Si-O sont rigides et directionnelles. En revanche, l’angle Si-O-Si est flexible, les possibilités d’arranger les tétraèdres entre eux sont donc très variées. La silice se présente sous différentes formes cristallines, basées sur différents enchaînements des tétraèdres. Elle peut aussi se présenter sous une forme totalement amorphe, lorsque le réseau de tétraèdres (ou « réseau silicaté ») n’a pas d’ordre périodique à longue distance : elle est alors un verre. Sur l’image de droite obtenue par microscopies à champ proche d’une monocouche de silice, on voit le passage de l’ordre cristallin (à gauche) au verre (à droite).
L’énergie interne élevée et la structure atomique compacte ont un lien direct aux propriétés:
- Les températures de fusion sont élevées : les matériaux céramiques sont réfractaires. Avec les oxydes, il faut aller à 1000°C ou plus pour obtenir de la mobilité atomique, de la réactivité, des débuts de transformation. Les températures de fusion sont, selon les compositions, de 900°C à plus de 2700°C (cas de la zircone, ZrO2).
- Ce sont des matériaux rigides et durs. Leur module d’Young est très élevé.
- Ce sont des matériaux fragiles, et qui résistent généralement mal au choc thermique. Le réseau de liaisons iono-covalentes s’oppose au déplacement de dislocations, de sorte que la plasticité est quasi-nulle. La rupture est donc brutale, et fortement liée à la présence de défauts qui concentrent les contraintes (microfissures…). En cas de choc thermique, la contrainte liée à la variation de volume (dilatation) peut suffire à casser la pièce.
Dans la liaison iono-covalente, les électrons de valence sont fortement localisés, soit sur l’anion (cas ionique), soit entre les 2 atomes (cas covalent). En conséquence ces composés sont non conducteurs électroniques, ce sont des « diélectriques ». Mais ils peuvent être conducteurs ioniques, selon la mobilité des ions dans le réseau cristallin.
La réfractarité, la rigidité et les propriétés diélectriques des céramiques sont à l’origine de leurs applications comme matériaux de structure, chimiquement inertes et isolants, comme réfractaires dans l’industrie, comme matériaux de découpe ou d’abrasion, et comme composants diélectriques. Les chimistes font beaucoup d’efforts pour relever les deux points faibles : la résistance mécanique et la résistance au choc thermique. Cela passe par le contrôle fin de la microstructure.
Microstructure et propriétés mécaniques des céramiques
Comme vous le savez, on contrôle la microstructure par le procédé d’élaboration. Les céramiques techniques telles que Al2O3, SiC, … sont obtenues par frittage d’une poudre compactée. Lors du traitement thermique de frittage, les grains cristallins vont croître et se lier les uns aux autres en développant les joints de grains et en diminuant la porosité. A la fin, le matériau est polycristallin avec des cristaux plus ou moins gros et polydisperses, de la porosité résiduelle, et éventuellement des impuretés (cristallines ou vitreuses) situées dans les joints de grain.
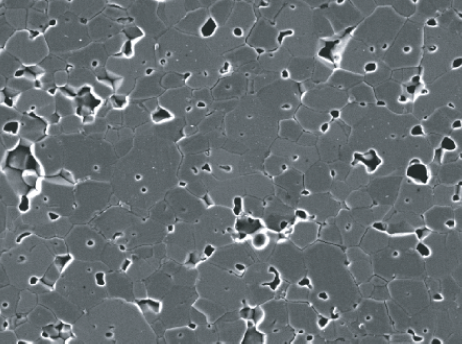
Microstructure typique d’une céramique (image MEB, électrons secondaires). La taille des grains et des pores est de l’ordre de 10 µm.
Les céramiques traditionnelles ont une façon un peu différente de se consolider lors de la cuisson: elles développent une phase liquide, plus ou moins abondante selon la composition et la température. Les forces capillaires dans la phase liquide vont provoquer le réarrangement des grains et la diminution de la porosité. Lors du refroidissement, la phase liquide va se vitrifier. Elle forme un liant entre les cristaux, on parle de « céramiques vitrifiées ». Les terres cuites frittent quasiment sans phase liquide, elles sont par conséquent très poreuses. Les faïences sont peu vitrifiées et sont poreuses. Les grès sont un peu plus vitrifiés et plus denses, et les porcelaines sont très vitrifiées et denses : dans leur cas la phase vitreuse peut même devenir majoritaire.
[microstructure d’une terre cuite, d’une faïence et d’une porcelaine]
De façon générale, plus la céramique est poreuse, moins elle est résistante mécaniquement. C’est pour cela que les terres cuites et les faïences sont plus épaisses que le grès ou la porcelaine : l’épaisseur est une façon d’augmenter la résistance mécanique (la fracture a plus de matière à traverser). Dans les céramiques techniques, on va essayer d’obtenir une microstructure homogène avec un minimum de porosité résiduelle, en optimisant la composition et le traitement de frittage de façon à accélérer les processus de densification.
Les verres
Les céramiques traditionnelles (faïences, grès…) sont constituées de phases cristallines et d’une phase vitreuse aluminosilicates, obtenues par la transformation thermique d’un mélange d’argiles, de quartz et de feldspaths (des aluminosilicates alcalins ou alcalino-terreux qui ont un rôle de fondants). Si on augmente la proportion de feldspaths, ou qu’on ajoute des oxydes très « fondants » tels que des oxydes alcalins ou alcalino-terreux, on va réussir à fondre complètement le mélange. Une fois le liquide silicaté homogénéisé, il suffit de le refroidir rapidement pour l’empêcher de cristalliser et obtenir un verre. Le verre est aussi homogène et exempt de microdéfauts (joints de grains, porosité) que l’est n’importe quel liquide. Il est donc transparent comme un liquide, mais c’est bien un solide : les atomes dans le verre ne bougent pas les uns par rapport aux autres, ils ne font que vibrer autour de leur position d’équilibre.
Les verres courants sont des verres silicatés obtenus à partir d’un mélange principalement de sable (SiO2) et de fondants (Na2O, K2O, CaO, MgO). Lors du chauffage, les fondants réagissent avec la silice pour former des silicates alcalins à bas point de fusion, comme indiqué dans les diagrammes de phase. On obtient un verre « silicate alcalin ». Pour améliorer les propriétés physiques et chimiques, il est possible de modifier la composition en ajoutant d’autres oxydes (B2O3, Al2O3, ZrO2, …).
Les vitrocéramiques
Les liants hydrauliques
